 Maxime Jacoupy, Directeur Data à l’Institut de Myologie, pilote la plateforme MyoData. Docteur en neurosciences et diplômé d’un master en intelligence artificielle, il incarne une double compétence à l’interface des sciences biomédicales et des technologies numériques.
Maxime Jacoupy, Directeur Data à l’Institut de Myologie, pilote la plateforme MyoData. Docteur en neurosciences et diplômé d’un master en intelligence artificielle, il incarne une double compétence à l’interface des sciences biomédicales et des technologies numériques.
Sa mission : structurer, fiabiliser et rendre exploitables les données produites à tous les niveaux au sein de l’Institut.
Votre parcours mêle à la fois biologie et data science, en quoi cette double formation est essentielle ?
M.J. Je suis chercheur, avec une formation complémentaire en data science/intelligence artificielle. L’objectif de la plateforme MyoData est de concevoir des outils à la fois utiles, fiables et compréhensibles par les chercheurs. Pour cela, il faut maîtriser plusieurs langages : ceux de la biologie, de l’algorithmie et des mathématiques. La méthodologie d’analyse peut s’acquérir, mais une base scientifique solide reste indispensable.
Comment se structure l’action de MyoData à l’échelle de l’Institut ?
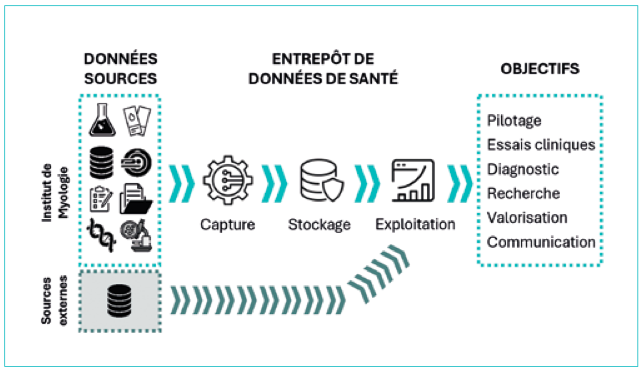 M.J. L’activité de l’équipe repose sur deux volets. Le premier est analytique : les chercheurs, médecins, ingénieurs sont accompagnés dans le traitement de leurs données, qu’il s’agisse de statistiques, de bioinformatique ou de développement d’algorithmes. Le second est structurel : une base de données globale, l’Entrepôt de Données (EDS) MyoData, est en cours de développement pour centraliser les données de l’Institut issues de la recherche clinique, des laboratoires et du soin. L’EDS constitue un socle transversal, sécurisé et conforme aux exigences de la certification Hébergeurs de Données de Santé (HDS) qui permettra la réalisation de nouvelles recherches sur ces données.
M.J. L’activité de l’équipe repose sur deux volets. Le premier est analytique : les chercheurs, médecins, ingénieurs sont accompagnés dans le traitement de leurs données, qu’il s’agisse de statistiques, de bioinformatique ou de développement d’algorithmes. Le second est structurel : une base de données globale, l’Entrepôt de Données (EDS) MyoData, est en cours de développement pour centraliser les données de l’Institut issues de la recherche clinique, des laboratoires et du soin. L’EDS constitue un socle transversal, sécurisé et conforme aux exigences de la certification Hébergeurs de Données de Santé (HDS) qui permettra la réalisation de nouvelles recherches sur ces données.
Vous êtes également impliqué dans GenoTher, biocluster dédié aux thérapies du gène. Quel est votre rôle dans cette structure ?
M.J. À travers l’EDS MyoData, nous interviendrons dans la phase d’analyse des données pré- et post-essai. L’objectif est de développer des outils permettant d’évaluer l’efficacité des traitements, d’anticiper la réponse des patients, ou encore de limiter le recours à des “bras témoins”. Ces travaux reposent sur des approches combinant intelligence artificielle et modélisation statistique.
Quel avenir voyez-vous pour ces pratiques ?
M.J. L’analyse des données est déjà très avancée en oncologie. Dans les maladies rares, il reste du chemin à parcourir, mais c’est précisément ce qui rend le travail passionnant. Dès lors que les données sont bien structurées et accessibles, ces approches peuvent transformer en profondeur la manière de produire des connaissances et d’accompagner les patients.
